Small:重庆大学王槐志等团队合作研究发现铜-锰基纳米材料诱导铜死亡并增强抗肿瘤免疫反应
2025-02-28 iNature iNature 发表于陕西省
该研究开发了一个新型Cu2O-MnO@PEG(CMP)纳米材料,用于肿瘤治疗。CMP直接介导肿瘤细胞的铜死亡,增强肿瘤微环境(TME)中的抗肿瘤免疫反应以诱导肿瘤消退。
癌症发病率不断上升,但大多数接受传统治疗的恶性癌症患者会出现肿瘤复发和短期5年生存率。
2025年2月16日,重庆大学王槐志、蔡磊、Sun Pijiang和重庆医科大学吴忠均共同通讯在Small 在线发表题为“A Copper-Manganese Based Nanocomposite Induces Cuproptosis and Potentiates Anti-Tumor Immune Responses”的研究论文。该研究开发了一个新型Cu2O-MnO@PEG(CMP)纳米材料,用于肿瘤治疗。CMP直接介导肿瘤细胞的铜死亡,增强肿瘤微环境(TME)中的抗肿瘤免疫反应以诱导肿瘤消退。
CMP改善树突状细胞和肿瘤相关巨噬细胞的肿瘤抗原加工和呈递,并进一步促进CD8+ T细胞反应,尤其是细胞毒性CD8+ T细胞和暂时衰竭CD8+ T细胞。此外,CMP下调Treg细胞的比例和Treg细胞上的CTLA-4表达。CMP诱导针对远端肿瘤和长期免疫记忆的全身免疫反应,与PD-L1mAb协同作用抑制肿瘤,并维持PD-L1mAb治疗后的抗肿瘤疗效。总得来说,该策略能够协同促进肿瘤细胞的铜死亡和抗肿瘤免疫反应,具有临床治疗潜力。

随着发病率和死亡率的增加,癌症成为全球最重要的健康问题之一。消除癌症的传统疗法是手术、化疗和放疗。除传统疗法外,癌症免疫疗法也受到了越来越多的关注。然而,部分高度致死性或难治性癌症患者预后较差,短期5年生存率低。因此,需要进一步探索癌症治疗的新策略。
铜在许多细胞生物过程中起着至关重要的作用。此外,铜还与各种癌症类型相关。铜死亡是一种新的铜依赖性细胞死亡形式,与细胞凋亡、焦亡、坏死性凋亡和铁死亡等已知的细胞死亡形式不同。铜与三羧酸(TCA)循环中的硫辛酰化蛋白结合并降低铁硫(Fe-S)簇蛋白水平来触发细胞死亡,能够介导肿瘤根除。
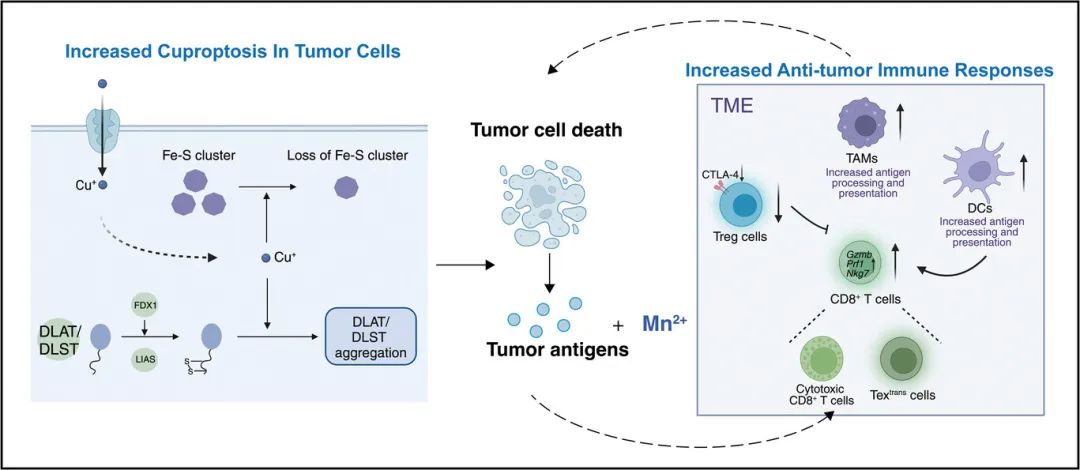
图1 CMP治疗肿瘤示意图(摘自Small )
肿瘤细胞死亡后,抗原呈递细胞(APC)释放肿瘤抗原,并被巨噬细胞和树突状细胞(DC)摄取,加工肿瘤抗原并将其呈递给CD8+ T细胞和CD4+ T细胞,以介导肿瘤抑制。然而,肿瘤细胞释放的免疫原性较低的抗原不能引发有效的抗肿瘤反应,以介导已建立肿瘤的肿瘤消退。因此,有必要开发能够促进抗原免疫原性、塑造肿瘤微环境(TME)和减少抗原量以增强抗肿瘤功效的佐剂。据报道,锰可增强巨噬细胞和树突状细胞的肿瘤抗原呈递,并增强CD8+ T细胞应答。锰和PD-1抗体的组合表现出良好的抗肿瘤作用。结果表明,锰可能成为一种有效的癌症治疗辅助手段。
该研究开发了Cu2O-MnO@PEG(CMP)探索其在体外和体内不同类型肿瘤中的抗肿瘤活性。作者假设CMP中的铜可以直接诱导肿瘤细胞铜死亡。同时,锰与肿瘤细胞铜死亡释放的肿瘤抗原结合,诱导强大的抗肿瘤免疫反应。此外,作者评估了CMP与PD-L1阻断协同作用是否可以作为癌症治疗的替代策略。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/smll.202412174
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#铜死亡# #抗肿瘤免疫反应#
14